Sabões e Detergentes
Lista de 18 exercícios de Química com gabarito sobre o tema Sabões e Detergentes com questões de Vestibulares.
01. (UFPR) A utilização de sabões para limpeza data de mais de 4000 anos. Os sabões são constituídos de moléculas anfifílicas, que contêm uma porção hidrofóbica e uma hidrofílica, e consequentemente atuam como tensoativos. Além da ação física do sabão no processo de remoção de sujeiras, há também a ação química, em que ocorre reação entre as moléculas anfifílicas e a sujeira, principalmente gorduras. Mesmo sem conhecimento científico, muitas pessoas constatam que a lavagem com sabão utilizando água quente é mais eficiente que com água fria. Com relação à ação dos sabões, considere as seguintes afirmativas:
1. A velocidade de remoção de sujeiras (à base de gorduras) de uma roupa é aumentada em altas temperaturas, pois nessa condição há maior frequência de choques entre as moléculas.
2. O processo de solubilização da sujeira envolve interação entre a parte hidrofóbica do tensoativo e a gordura, deixando a parte hidrofílica exposta na superfície que interage com o solvente.
3. A maior eficiência de lavagem em temperaturas mais altas implica que a reação entre o tensoativo e a sujeira é um processo endotérmico.
4. Em temperaturas superiores à temperatura de fusão de gorduras da sujeira, a velocidade de remoção é aumentada, em função da maior superfície de contato.
Assinale a alternativa correta.
- Somente as afirmativas 1 e 2 são verdadeiras.
- Somente as afirmativas 1 e 3 são verdadeiras.
- Somente as afirmativas 1, 2 e 4 são verdadeiras.
- Somente as afirmativas 2, 3 e 4 são verdadeiras.
- As afirmativas 1, 2, 3 e 4 são verdadeiras.
02. (UFPR) A dureza da água é um problema que afeta residências e indústrias por gerar acúmulo mineral nas tubulações e dificultar a formação de espumas de sabão e detergentes. Relacione os elementos da coluna da esquerda, que apresenta as constantes de produto de solubilidade de carbonatos, com as afirmativas da coluna da direita.

Assinale a alternativa que apresenta a numeração correta da coluna da direita, de cima para baixo.
- 3 – 4 – 1 – 2.
- 3 – 2 – 1 – 4.
- 4 – 2 – 3 – 1.
- 3 – 1 – 4 – 2.
- 2 – 4 – 1 – 3.
03. (UniAtenas) Sabão é um produto tensoativo usado em conjunto com a água para lavar e limpar. Do ponto de vista químico são obtidos pela hidrólise alcalina de glicerídeos (gorduras). A reação química desse processo é denominada saponificação, gorduras e bases são hidrolisadas em água: Éster + base → sal orgânico + álcool
Sobre esse assunto são feitas afirmações:
I. O sabão emulsiona o óleo, que constitui a sujeira, podendo ser prejudicado pela “água dura” (contém sais de Ca++) dando origem a precipitados.
II. Sabões são substâncias sufarctantes com propriedades anfifílicas, ou seja, apresenta em suas moléculas parte polares e partes apolares.
III. Detergentes são compostos por moléculas de baixo peso molecular, geralmente sais de ácidos sufônicos, apresentando extremidades com caráter diferentes de polaridades.
IV. Detergentes apresentam “vantagens” em relação aos sabões, são biodegradáveis e mantêm eficazes mesmo em “água dura”, pois os sais correspondentes são solúveis.
Das assertivas expostas é correto apenas o que se afirmar em:
- I;
- I e II;
- II;
- III e IV;
- I, II, III e IV.
04. (UNIFOR) Se fossemos usar somente água para remover certos tipos de sujeira, por exemplo, manchas de óleos ou gorduras, certamente a limpeza não seria tão eficiente. No entanto, os sabões e detergentes apresentam melhor eficiência na limpeza porque possuem substâncias cujas estruturas apresentam:
- grupos apolares que se ligam a sujeira (óleo), facilitando sua remoção.
- grupos polares que se ligam a sujeira (óleo), facilitando sua remoção.
- grupos polares capazes de reagirem com a água e apolares que se ligam a sujeira, facilitando sua remoção.
- grupos apolares capazes de reagirem com a água e polares que se ligam a sujeira (óleo), facilitando sua remoção.
- grupos iônicos, nas extremidades, capazes de reagirem com a água e a sujeira, facilitando sua remoção.
05. (Fuvest) Leia o seguinte texto:
Era o que ele estudava. “A estrutura, quer dizer, a estrutura” — ele repetia e abria as mãos branquíssimas ao esboçar o gesto redondo. Eu ficava olhando seu gesto impreciso porque uma bolha de sabão é mesmo imprecisa, nem sólida nem líquida, nem realidade nem sonho. Película e oco. “A estrutura da bolha de sabão, compreende?” Não compreendia. Não tinha importância. Importante era o quintal da minha meninice com seus verdes canudos de mamoeiro, quando cortava os mais tenros que sopravam as bolas maiores, mais perfeitas. Lygia Fagundes Telles, A estrutura da bolha de sabão, 1973. A “estrutura” da bolha de sabão é consequência das propriedades físicas e químicas dos seus componentes. As cores observadas nas bolhas resultam da interferência que ocorre entre os raios luminosos refletidos em suas superfícies interna e externa. Considere as afirmações abaixo sobre o início do conto de Lygia Fagundes Telles e sobre a bolha de sabão:
I. O excerto recorre, logo em suas primeiras linhas, a um procedimento de coesão textual em que pronomes pessoais são utilizados antes da apresentação de seus referentes, gerando expectativa na leitura.
II. Os principais fatores que permitem a existência da bolha são a força de tensão superficial do líquido e a presença do sabão, que reage com as impurezas da água, formando a sua película visível.
III. A ótica geométrica pode explicar o aparecimento de cores na bolha de sabão, já que esse fenômeno não é consequência da natureza ondulatória da luz. Está correto apenas o que se afirma em
- I.
- I e II.
- I e III.
- II e III.
- III
06. (Acafe-SC) No jornal Folha de São Paulo, de 23 de junho de 2015, foi publicada uma reportagem sobre a formação de espuma branca no rio Tietê ´´[…] a formação de espuma está associada à baixa vazão da água e à presença de esgoto doméstico não tratado. A falta de oxigênio na água dificulta a degradação de detergente doméstico […]”.
Baseado nas informações fornecidas e nos conceitos químicos, analise as afirmações a seguir.
I. O detergente é uma substância anfipática.
II. O complexo formado entre detergente, óleo e água pode ser chamado de micela.
III. O oxigênio é uma molécula apolar formada por uma ligação covalente do tipo sigma (σ) e outra do tipo pi (π).
IV. A espuma branca formada pode ser classificada de coloide.
Assinale a alternativa correta:
- Apenas I, II e III estão corretas.
- Apenas II, III e IV estão corretas.
- Todas as afirmações estão corretas.
- Apenas a afirmação IV está correta.
07. (EBMSP) Os compostos químicos que constituem o sabão e os detergentes conseguem interagir com substâncias polares e apolares, o que contribui para a limpeza de objetos e superfícies. A diferença entre esses dois materiais está na estrutura molecular das substâncias químicas constituintes, sendo que o sabão é formado por sais de ácidos carboxílicos de cadeia longa — estrutura I — e os detergentes, geralmente, são produzidos a partir de sais derivados de ácidos sulfônicos de cadeia longa — estruturas II e III. Além disso, o tipo de cadeia carbônica do composto orgânico influencia na decomposição da substância química por micro-organismos, sendo os compostos orgânicos representados por I e II biodegradáveis e o composto III não biodegradável.

Com base nessas informações e nas estruturas desses compostos químicos, é correto afirmar:
- A parte hidrófoba do sabão representado em I associa-se a moléculas de água por ligações de hidrogênio.
- O composto químico representado em II apresenta como parte hidrófila a extremidade polar representada por — SO ‾3.
- A existência da cadeia carbônica ramificada na estrutura do detergente contribui para a decomposição da substância química por micro-organismos.
- O hidrogênio do benzeno, matéria-prima para a fabricação dos detergentes, é substituído por um radical alquil representado por — C12H23 na estrutura III.
- A substância química representada em I é obtida pela reação entre o ácido decanoico, C9H19COOH(aq), e a solução aquosa de cloreto de sódio, NaCl(aq).
08. (FCM-MG) Sabões são sais de ácidos graxos, como o estearato de sódio – C17H35COONa –, ao passo que detergentes são sais de sódio de alcoóis sulfatados de longa cadeia, como o lauril sulfato de sódio (C11H23CH2OSO3Na). A água dura, que contém cátions cálcio e magnésio, reage com o sabão, formando sabões insolúveis. Entretanto, forma sais solúveis com os detergentes. Analisando essas informações e utilizando seus conhecimentos, não podemos afirmar que:
- detergentes e sabões contêm uma parte polar (hidrófila) e uma parte apolar (hidrofóbica).
- em água dura, há necessidade de mais sabão para se produzir espuma que em água de menor dureza.
- estearato de sódio é um sabão proveniente da saponificação de um óleo, ou seja, de um ácido graxo insaturado.
- lauril sulfato de sódio pode ser preparado a partir de um álcool de 12 carbonos com ácido sulfúrico, seguido de uma neutralização com hidróxido de sódio.
09. (UnP) A fabricação de sabão para limpeza é conhecida há séculos e narrada pelos antigos historiadores. Com o progresso rápido na indústria durante os séculos XIX e XX, a fabricação de sabão mudou um pouco e a maior parte produzida hoje é pelo chamado processo contínuo. Usado principalmente para fins de lavagens e como agente emulsionante, o sabão consiste principalmente de hidróxidos de sódio ou potássio e de ácidos gordurosos. Os sabões produzidos a partir de hidróxido de sódio (soda cáustica) são conhecidos como “sabões duros”, já os fabricados a partir de hidróxido de potássio são conhecidos como “sabões moles”. Outros tensoativos, frequentemente conhecidos como detergentes sintéticos, competem com os sabões em muitos usos. Um sabão pode ser preparado pelo aquecimento da banha de porco com soda cáustica. Esse tipo de sabão, quando usado com águas contendo sais de cálcio e magnésio, forma um precipitado.
Considere as afirmações a seguir:
I – Sais do tipo carboxilato de cálcio com cadeias longas são solúveis.
II – A molécula de sabão é constituída de uma parte hidrofílica e outra hidrofóbica.
III – A parte hidrofóbica do sabão é sua cadeia orgânica.
IV – A parte hidrofílica do sabão é o grupo carboxilato.
Pode-se afirmar que:
- Somente as afirmativas I e IV são verdadeiras.
- Somente as afirmativas II e III são verdadeiras.
- Somente as afirmativas II, III e IV são verdadeiras.
- Somente as afirmativas I e II são verdadeiras.
10. (UNCISAL) Quando se utiliza sabões/detergentes biodegradáveis em processos de lavagem industrial ou doméstico, estes podem chegar aos lagos e rios através do sistema de esgoto. Neste caso, os resíduos são degradados pela ação de microrganismos que produzem enzimas capazes de deteriorar moléculas de cadeias carbônicas lineares. Porém, estas enzimas não reconhecem moléculas de cadeias ramificadas.
Spiro, T.G. e Stigliani, W.M. Química Ambiental. São Paulo: Pearson, 2009 (adaptado)
Considerando os benefícios ao ambiente, qual composto pode ser classificado como biodegradável?
11. (PUC-RS) O dodecilbenzeno, cuja estrutura é representada por

é matéria-prima do tensoativo mais utilizado na fabricação de detergentes domésticos. Tendo baixo custo e boa biodegradabilidade, é excelente agente emulsionante.
O dodecilbenzeno é um
- alceno de massa molar igual a 246g.
- composto com doze átomos de carbono na parte linear e cinco átomos de carbono na parte cíclica da cadeia.
- composto aromático de fórmula mínima C5H3 .
- hidrocarboneto de fórmula molecular C18H30.
- alcano de cadeia carbônica mista.
12. (UECE) É conhecida como água dura um tipo de água que contém sais de cálcio e magnésio dissolvidos. Esse tipo de água forma pouca espuma quando usada com sabão comum para lavar roupas e produz incrustações nas paredes de dutos e equipamentos. O procedimento que minimiza a ação da água dura é a
- filtração.
- desmineralização.
- sublimação.
- decantação.
13. (UECE) Para que uma horta produza bons legumes e frutas, é necessário que ela esteja distante de árvores e livre de pedras e insetos. No combate aos insetos, devem ser aplicadas soluções aquosas de sabão, puras ou com querosene. No que diz respeito a estas substâncias, assinale a afirmação verdadeira.
- Sabão é uma substância orgânica pertencente à família dos hidrocarbonetos.
- Querosene é obtido do petróleo, que pertence à família dos alcenos.
- Sabão é formado por moléculas que possuem uma cadeia carbônica longa, apolar, contendo o grupo carboxílico, que é polar, e, portanto, solúvel em água.
- Querosene é uma mistura de alcanos que possuem cadeias carbônicas contendo de 6 a 10 átomos de carbono (C6 a C10).
14. (UNICAMP) Uma prática de limpeza comum na cozinha consiste na remoção da gordura de panelas e utensílios como garfos, facas, etc. Na ação desengordurante, geralmente se usa um detergente ou um sabão. Esse tipo de limpeza resulta da ação química desses produtos, dado que suas moléculas possuem
- uma parte com carga, que se liga à gordura, cujas moléculas são polares; e uma parte apolar, que se liga à água, cuja molécula é apolar.
- uma parte apolar, que se liga à gordura, cujas moléculas são apolares; e uma parte com carga, que se liga à água, cuja molécula é polar.
- uma parte apolar, que se liga à gordura, cujas moléculas são polares; e uma parte com carga, que se liga à água, cuja molécula é apolar.
- uma parte com carga, que se liga à gordura, cujas moléculas são apolares; e uma parte apolar, que se liga à água, cuja molécula é polar.
15. (UEG) A remoção de gordura em utensílios domésticos é feita por ação mecânica, entretanto, a ação dos sabões facilita o processo de remoção de sujeiras gordurosas. Um exemplo de uma molécula de sabão é o dodecanoato de sódio, cuja estrutura química está mostrada a seguir.

O papel do sabão no processo de limpeza ocorre devido à
- interação de van der Walls da parte apolar e à ligação de hidrogênio da parte polar de sua molécula, respectivamente, com a gordura e a água.
- redução do pH do meio, possibilitando a solubilização da gordura na água.
- diminuição da densidade da água, facilitando a precipitação das moléculas de gordura, que serão removidas por centrifugação.
- tensão superficial da água que é elevada e que possibilita a formação de espuma que remove a sujeira.
16. (UNESP) Até hoje o corpo humano é um enorme depósito de gorduras. Até uma pessoa magra, de 1,80 m de altura e 70 kg, carrega consigo, em média, cerca de um quinto de seu peso em forma de gordura; ou seja, 14 quilos. (...) Independente de como esse material está distribuído, ele sempre é constituído do mesmo tipo de célula - o adipócito ou célula adiposa. (...) Programados para se depositarem, os adipócitos vão juntando gradualmente os blocos de construção básica que formam a gordura: os ácidos graxos. Cada três deles constroem um chamado triglicerídeo, uma minúscula molécula de gordura que é armazenada pelas células (...).
(Revista Geo, n. 38. p. 47)
Na reação de saponificação de um triglicerídeo há produção do sabão e de
- etanol.
- formol.
- água.
- soda cáustica.
- glicerol.
17. (UFPR) A utilização de sabões para limpeza data de mais de 4000 anos. Os sabões são constituídos de moléculas anfifílicas, que contêm uma porção hidrofóbica e uma hidrofílica, e consequentemente atuam como tensoativos. Além da ação física do sabão no processo de remoção de sujeiras, há também a ação química, em que ocorre reação entre as moléculas anfifílicas e a sujeira, principalmente gorduras. Mesmo sem conhecimento científico, muitas pessoas constatam que a lavagem com sabão utilizando água quente é mais eficiente que com água fria. Com relação à ação dos sabões, considere as seguintes afirmativas:
1. A velocidade de remoção de sujeiras (à base de gorduras) de uma roupa é aumentada em altas temperaturas, pois nessa condição há maior frequência de choques entre as moléculas.
2. O processo de solubilização da sujeira envolve interação entre a parte hidrofóbica do tensoativo e a gordura, deixando a parte hidrofílica exposta na superfície que interage com o solvente.
3. A maior eficiência de lavagem em temperaturas mais altas implica que a reação entre o tensoativo e a sujeira é um processo endotérmico.
4. Em temperaturas superiores à temperatura de fusão de gorduras da sujeira, a velocidade de remoção é aumentada, em função da maior superfície de contato.
Assinale a alternativa correta.
- Somente as afirmativas 1 e 2 são verdadeiras.
- Somente as afirmativas 1 e 3 são verdadeiras.
- Somente as afirmativas 1, 2 e 4 são verdadeiras.
- Somente as afirmativas 2, 3 e 4 são verdadeiras.
- As afirmativas 1, 2, 3 e 4 são verdadeiras.
18. (PUC-RS) INSTRUÇÃO: Para responder à questão, analise o texto a seguir.
O sabão é um dos produtos químicos de maior importância no cotidiano. É produzido a partir de óleos e gorduras de origem vegetal ou animal e, na maioria das vezes, constitui-se dos sais de sódio ou potássio derivados de ácidos graxos. A estrutura abaixo é típica de sabões:
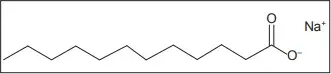
Embora o sabão seja muito solúvel em meio aquoso, é possível diminuir sua solubilidade.
Uma forma efetiva de diminuir a quantidade de sabão dissolvido é adicionar certos compostos à solução. Dois exemplos são:
- açúcar e sal de cozinha.
- sal de cozinha e ácido de bateria.
- ácido de bateria e amoníaco.
- amoníaco e água.
- água e açúcar.




