Cetonas
Lista de 15 exercícios de Química com gabarito sobre o tema Cetonas com questões de Vestibulares.
01. (Unifor) As cetonas são formadas por átomos de carbono, hidrogênio e:
- Oxigênio.
- Nitrogênio.
- Halogênio.
- Enxofre.
02. (Cesgranrio-RJ) Dentre os compostos:
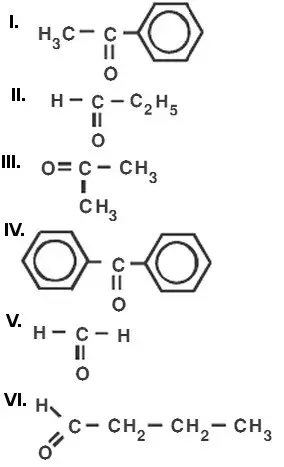
pertencem à função cetona:
- apenas I, III e IV.
- apenas I, IV e V.
- apenas II, III e IV.
- apenas II, IV e V.
- apenas II, V e VI.
03. (UFRO) A fórmula H3C—CO—CH2—CH3 corresponde ao composto:
- Ácido butanóico.
- Butanol.
- Butanal.
- Butanona.
- Etóxi-etano.
04.(Fuvest-SP)
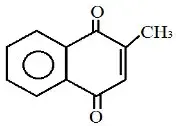
Na vitamina K3 (fórmula acima), reconhece-se o grupo funcional:
- ácido carboxílico.
- aldeído.
- éter.
- fenol.
- cetona.
05. (U. Católica de Salvador – BA) A cetona é um composto carbonílico com 3 átomos de carbono e cadeia saturada. Sua fórmula molecular é:
- C3H6O
- C3H7O
- C3H8O
- C3H8O2
- C3H8O3
06. (Unirio) A Medical Association relacionou a terapia de reposição hormonal pós-menopausa ao aumento do risco de desenvolvimento de câncer de mama, pois os hormônios alteram as características dos tumores e atrasam, assim, o diagnóstico da doença.
Há dois tipos distintos de hormônios sexuais femininos, sendo um deles a progesterona, cuja estrutura apresenta um grupo funcional correspondente à função:
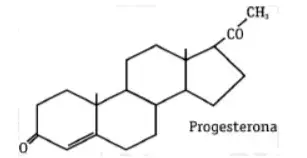
- Ácido carboxílico.
- Cetona.
- Éster.
- Álcool.
07. (UFRO) A fórmula H3C-CO-CH2-CH3 corresponde ao composto
- ácido butanóico
- butanol
- butanal
- butanona
- etóxi-etano
08. (UFMG) Cetonas macrocíclicas são usadas em perfumes porque possuem intenso cheiro de almíscar e retardam a evaporação de constituintes mais voláteis.
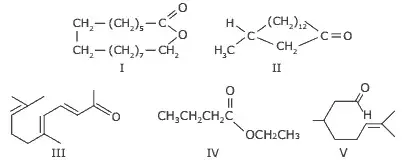
A identificação CERTA das estruturas de substâncias com cheiro de almíscar é:
- I, II, III, IV e V.
- II, III e V.
- I e II.
- I e IV.
- II.
09. (UNIVAG) A acetona (CH3COCH3) pode ser obtida pela oxidação parcial do composto
- CH3CH2CH2OH
- CH3CH2COOH
- CH3CH(OH)CH3
- CH3COOCH3
- CH3CH2CHO
10. (UEFS) O isopropanol (massa molar = 60 g/mol) é um álcool muito utilizado como solvente para limpeza de circuitos eletroeletrônicos. A produção mundial desse álcool chega a 2,7 milhões de toneladas por ano. A indústria química dispõe de diversos processos para a obtenção de isopropanol, entre eles, o que envolve a reação de acetona (massa molar = 58 g/mol) com hidrogênio. A equação dessa reação é
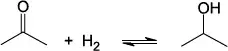
A transformação de acetona em isopropanol é uma reação orgânica em que a acetona sofre
- hidrólise.
- substituição.
- hidratação.
- redução.
- esterificação.
11. (Unaerp) Cães farejadores são usados para detectar a presença de drogas em bagagens nos aeroportos. Sabendo que a cocaína é um composto sólido contaminado por alguns solventes usados em sua purificação, entre eles a acetona (propanona), e que os cães conseguem farejar com mais facilidade a acetona do que a cocaína, conclui-se que esse composto deve ser
- menos volátil que a cocaína, com menor pressão de vapor.
- mais volátil que a cocaína, com menor pressão de vapor.
- menos volátil que a cocaína, com maior pressão de vapor.
- mais volátil que a cocaína, com maior pressão de vapor.
- mais volátil que a cocaína, sendo a pressão de vapor a mesma para as duas substâncias.
12. (UFPR) As cetonas pertencem a uma classe de substâncias empregadas como reagente de partida na síntese de outros compostos orgânicos, contendo diferentes grupos funcionais. No esquema abaixo, estão indicadas cinco rotas de síntese, as quais fornecem cinco produtos diferentes, a partir de uma mesma cetona:
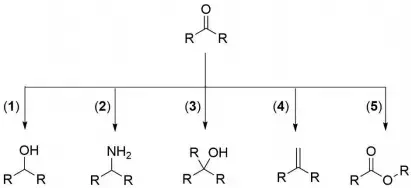
As rotas de síntese que geram produtos pertencentes a uma mesma classe de compostos orgânicos são:
- 1 e 2.
- 1 e 3.
- 2 e 4.
- 3 e 5.
- 4 e 5.
13. (UEL) O acetato de etila (CH3COOCH2CH3) é um éster simples, usado, no passado, como antiespasmódico e hoje como solvente industrial e removedor de esmalte de unha. A acetona (CH3(CO)CH3) também é usada como removedor de esmaltes, mas devido a sua elevada solubilidade em água, quando em contato com a pele, pode desidratá-la. Sabe-se que estes solventes possuem cheiros parecidos, tornando difícil a identificação pelo olfato.
Considerando um frasco contendo acetato de etila e acetona em quantidades equimolares, assinale a alternativa que apresenta, corretamente, o procedimento para a separação da mistura.
Dados:
Ponto de ebulição do acetato de etila a 1 atm =77,1 °C e densidade = 902 Kg/m³
Ponto de ebulição da acetona a 1 atm = 56,0 °C e densidade = 784 Kg/m³
- Empregar funil de separação, em que a acetona ficará na fase inferior do funil.
- Empregar destilação simples, pois a diferença dos pontos de ebulição dos solventes é elevada.
- Empregar destilação fracionada, em que o primeiro solvente a ser destilado será a acetona.
- Empregar destilação simples, pois se trata de uma mistura eutética, em que os solventes são imiscíveis.
- Empregar separação fracionada, aquecendo a mistura a 80 °C, sendo que o primeiro solvente a ser destilado será o acetato de etila.
14. (UEA) As cetonas são utilizadas como solventes orgânicos e se caracterizam por apresentarem numa cadeia carbônica o grupo funcional carbonila, com seu carbono secundário.
Considerando a cetona de menor massa molar, seu isômero plano de função pertence ao grupo funcional:
- amida.
- éster.
- aldeído.
- ácido carboxílico.
- éter.
15. (Fatec-SP) Na indústria de alimentos, sua aplicação mais importante relaciona-se à extração de óleos e gorduras de sementes, como soja, amendoim e girassol. À temperatura ambiente, é aldeidos.phpum líquido que apresenta odor agradável, e muito utilizado como solvente de tintas, vernizes e esmaltes. Trata-se da cetona mais simples.
O nome oficial e a fórmula molecular da substância descrita pelo texto anterior são, respectivamente:
- butanal e C4H8O.
- butanona e C4H7OH.
- etanona e C2H4O.
- propanal e C3H6O.
- propanona e C3H6O.